Leczenie zespołu stopy cukrzycowej to wyzwanie dla zespołu terapeutycznego. Skuteczna terapia ran powstałych na podłożu ZSC jest możliwa pod warunkiem zastosowania strategii TIME oraz dobranych do rany opatrunków specjalistycznych i skutecznych antyseptyków.
Opis przypadku dzięki uprzejmości mgr Magdaleny Mróz, gabinet leczenia ran Emmed Rzeszów
Opis przypadku
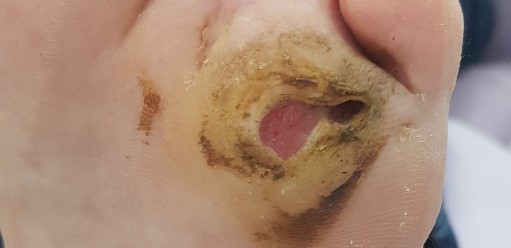
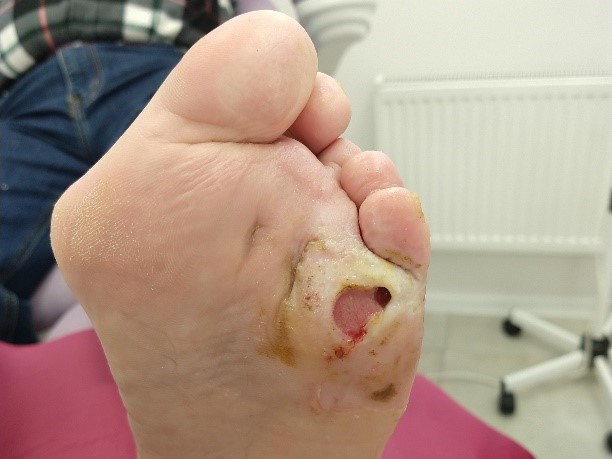
Pacjent w wieku 52 lat, chorujący na cukrzycę, z unormowaną glikemią, stan ogólny dobry. Zespół stopy cukrzycowej neuropatycznej z przetoką pod 5. głową kości śródstopia w okolicy podeszwowej stopy lewej. Rana o średnicy ok. 2 cm, drążąca w głąb kości śródstopia. Wokół rany liczne zrogowacenia, dno rany bladoróżowe, wyciek treści ropno-surowiczej. Rana z cechami infekcji, obecny przykry zapach z rany.
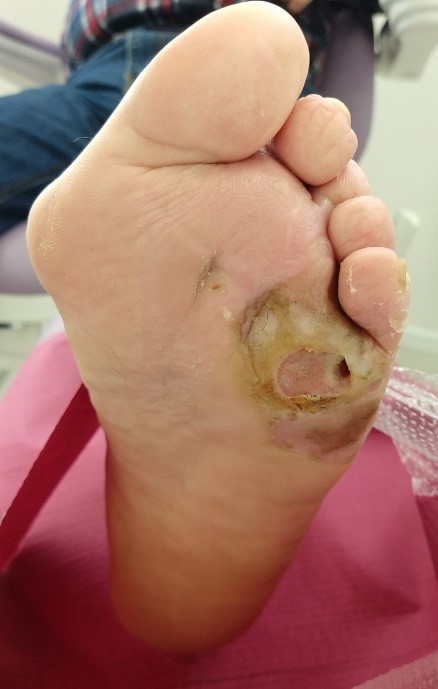
Leczenie w strategii TIME
W terapii zespołu stopy cukrzycowej zaleca się stosowanie strategii TIME. Podstawą terapii są następujące procedury: regularne oczyszczanie łożyska rany (etap T – Tissue debridement), kontrola obciążenia mikrobiologicznego, infekcji i zapalenia (etap I – Infection and inflammation control), zarządzanie raną w optymalnie wilgotnym środowisku (etap M – Moisture balance) oraz pielęgnacja brzegów rany i wspieranie procesu naskórkowania, czyli etap E (Edges, epidermization).
W opisanym przypadku w ramach strategii TIME podjęto następujące działania:
Etap T – wykonano łyżeczkowanie przetoki, usunięto tkanki hiperkeratotyczne z podeszwy stopy i przeprowadzono płukanie przetoki za pomocą roztworu Granudacyn®, który jest bezpiecznym produktem o szerokim spektrum działania przeciwdrobnoustrojowego. Produkt nie musi być wypłukiwany z łożyska rany.
Etap I – wykonano płukanie rany roztworem Granudacyn®. Przetokę zaopatrzono opatrunkiem Exufiber® Ag+ z zawartością siarczanu srebra. Opatrunek zabezpieczono pianką poliuretanową z siarczanem srebra i węglem aktywowanym Mepilex® Ag.
Etap M – dzięki odpowiednio dobranemu opatrunkowi stworzono wilgotne środowisko rany. Włókna alkoholu poliwinylowego, z których zbudowany jest opatrunek Exufiber® Ag+, charakteryzują się wysoką chłonnością, co sprawia, że skutecznie zatrzymują wysięk w swojej strukturze. Dzięki temu tkanki w obrębie przetoki oraz na podeszwie stopy nie były narażone na kontakt z wydzieliną z rany.
Etap E – usunięto hiperkeratozy z brzegów rany. Skórę wokół rany natłuszczono za pomocą maści Epaderm®.
Całość mocowano za pomocą bandaża kohezyjnego. Zmiana opatrunku odbywała się co 2-3 dni. Pacjentowi przekazano zalecenia dotyczące odciążania stopy za pomocą buta ortopedycznego (tzw. but gejszy).
Postępy w terapii
Po dwóch tygodniach terapii średnica rany zmniejszyła się o ok. 25% (z 2 cm do 1,5 cm). Zmniejszeniu uległa ilość wysięku surowiczego z rany. Nie stwierdzono obrzęku stopy ani cech infekcji. W dnie rany zaobserwowano czystą ziarninę.
Przetokę płukano preparatem Granudacyn® i zaopatrywano opatrunkiem Exufiber® Ag+. Jako opatrunek wtórny stosowano Mepilex® Ag. Całość mocowano za pomocą bandaża. Zmiana opatrunku następowała co 2-3 dni.
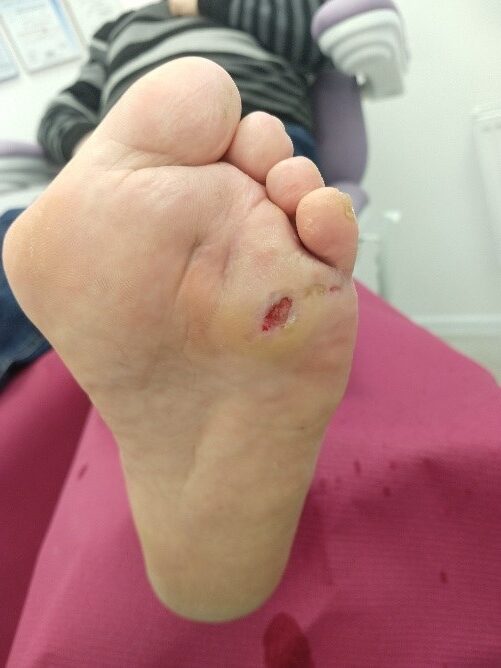
Po 45 dniach terapii przetoka uległa zagojeniu. Pozostała płytka rana o 0,5 cm średnicy. Na tym etapie leczenia przemywano ranę roztworem Granudacyn® i zabezpieczano opatrunkiem Mepilex®. Zmiana opatrunku odbywała się co 2 dni. Pacjentowi nadal zalecano odciążanie stopy.
Zalecenia dla pacjenta
Pacjentowi zalecono regularne pomiary glikemii i skierowano pod opiekę diabetologa. Ze względu na zaburzoną biomechanikę stopy (paluch koślawy i zmiana ciśnień wywieranych na podeszwę) pacjenta skierowano również do fizjoterapeuty, który po przeprowadzeniu indywidualnych badań podobarograficznych wykona indywidualne wkładki korygujące stopę. Pozwoli to zapobiec wystąpieniu ran w przyszłości.
Pacjentowi zalecono również wizyty u pielęgniarki podologicznej lub podologa. Podczas wizyt powinna być dokonywana kontrola stóp, usuwanie hiperkeratoz z podeszew stóp oraz oczyszczanie paznokci w sposób profesjonalny.
Efekt terapii na wagę złota
Skuteczność terapii ran trudno gojących się jest uzależniona od stosowania dobranych do potrzeb pacjenta opatrunków specjalistycznych oraz preparatów antyseptycznych.
Szczególnie ważnym elementem terapii ran z cechami infekcji jest płukanie ran bezpiecznym produktem o działaniu bójczym wobec drobnoustrojów, takim jak np. Granudacyn®.
Równie istotny jest prawidłowy dobór opatrunków. Opatrunek powinien się charakteryzować wysoką absorpcją i retencją, co zminimalizuje ryzyko przesiąkania opatrunku i maceracji tkanek. Jest to niezwykle istotne z uwagi na ograniczony przez epidemię dostęp pacjentów do opieki specjalistów w zakresie leczenia ran. Przykładem opatrunku, który charakteryzuje się wysoką chłonnością, jest żelujący opatrunek włóknisty Exufiber® Ag+. Co więcej, opatrunek ten wykazuje potwierdzone in vitro właściwości przekazywania wysięku do opatrunku wtórnego.
Dzięki zawartości siarczanu srebra opatrunek ten ma skuteczne działanie przeciwdrobnoustrojowe. Siarczan srebra eradykuje drobnoustroje już w ciągu 30 minut od aplikacji opatrunku. Właściwości bójcze utrzymują się nawet do 7 dni. Spektrum działania obejmuje bakterie Gram-dodatnie i Gram-ujemne, w tym również szczepy oporne na antybiotyki. Opatrunek Exufiber® Ag+jest zalecany przez międzynarodowe grupy eksperckie jako element postępowania przeciwbiofilmowego, uzupełniającego strategię TIME.
Opatrunek Exufiber® Ag+ cechuje ponadto spójna struktura, dzięki której jest on łatwy do wyjęcia w jednym kawałku nawet z głębokiej przetoki.

Wnioski
Terapia owrzodzeń w czasach pandemii może być utrudniona ze względu na rzadsze wizyty pacjentów w gabinecie chirurgicznym. Dlatego też poza edukacją pacjenta i jego rodziny niezwykle ważne jest stosowanie w terapii bezpiecznych rozwiązań, takich jak roztwór Granudacyn®, który może być stosowany do płukania ran, w tym również ran głębokich i przetok oraz tuneli, a także specjalistycznych opatrunków z siarczanem srebra, których stosowanie daje efekty na wagę złota.
Bibliografia:
- Dissemond J et al. Evidence for silver in wound care, meta-analysis of clinical studies from 2000–2015. J Dtsch Dermatol Ges. 2017 May;15(5):524-535.
2. Gee Kee E et al Randomized controlled trial of three burns dressings for partial thickness burns in children. Burns. 2015 Aug;41(5):946-55
3. Meaume S. et al. A study to compare a new self adherent soft silicone dressing with a self adherent polymer dressing in stage II pressure ulcers. Ostomy Wound Management, 2003.
4. Wiberg A.B. et al. Preventing maceration with a soft silicone dressing: in-vitro evaluations. Poster presented at the 3rd Congress of the WUWHS, Toronto, Canada, 2008.
5. Dhataryija K et al. An open, non comperative multicentre evaluation of performance and safety using an antimicrobial exudate transfer dressing on diabetic foot ulcers. A case series. J. Wound Care 2016; 25(5): 256–265.
6. Chadwick P, Taherinejad F, Hamberg K, Waring M. Clinical and scientific data on a silver-containing soft-silicone foam dressing: an overview. Journal of Wound Care 2009;18(11):483-491.
7. White R. et al. Evidence for atraumatic soft silicone wound dressing use. Wounds UK, 2005. 8. Gee Kee E et al. Cost-effectiveness of silver dressings for paediatric partial thickness burns: An economic evaluation from a randomized controlled trial. Burns. 2017 Jun;43(4):724-732.
9. Silverstein P. et al. Anopen, parallel, randomized, comparative, multicenter study to evaluate the cost-effectiveness, performance, tolerance, and safetyof a silver contain in soft silicone foam dressing vs silver sulfadiazine cream. J BurnCareRes. 2011 Nov-Dec; 32(6).
10. Zurcher S, Krapfl L, Burds A. Reducing postoperative surgical site infections in coronary artery bypass graft patients. Poster presentation at the 45th Annual Conference of the Wound Ostomy and Conti¬nence Nurses Society, Seattle, WA, US 2013.
11. Davis, S. C., Li, J. , Gil, J., Head, C., Valdes, J., Glinos, G. D., Solis, M. , Higa, A. and Pastar, I. (2019), Preclinical evaluation of a novel silver gelling fiber dressing on Pseudomonas aeruginosa in a porcine wound infection model. Wound Rep Reg, 27: 360-365
12. Gil et at. 2017. Evaluation of a Gelling Fiber Dressing with Silver to Eliminate MRSA Biofilm Infec¬tions and Enhance the Healing. Poster presented at the Symposium on Advanced Wound Care Spring meeting/Wound Healing Society (WHS) Annual Meeting 2017, Apr 05 – 09, 2017, San Diego, CA, USA.
13. Surgical Materials Testing Laboratory. BS EN 13726-1:2002: Test methods for primary wound dressings. Mölnlycke Health Care. Data on file. (2014).