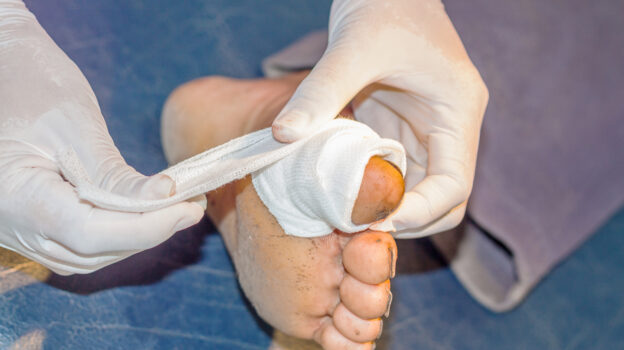
Infekcja bakteryjna jest powszechnym zjawiskiem w praktyce klinicznej. Rośnie liczba mutacji bakterii z tzw. grupy ESKAPE, które są odporne na antybiotyki. Dzięki współpracy naukowców Uniwersytetu Gdańskiego i Uniwersytetu w Tiencin powstała nowa metoda walki z wielolekoopornymi drobnoustrojami.
Blokowanie żelaza
W związku z rosnącą sprawnością mechanizmów molekularnych bakterii poddanych presji antybiotyków, naukowcy postanowili zmienić reguły gry. Efektem jest metoda, która polega na blokowaniu metabolizmu żelaza. Większość bakterii, które wywołują ludzkie choroby, aby żyć i rozmnażać się, potrzebuje tego pierwiastka. Dla bakterii żelazo jest kluczowym składnikiem odżywczym, niezbędnym do przetrwania i reprodukcji. Wspomaga enzymy m.in. w pośredniczeniu syntezy DNA, produkcji energii, transporcie tlenu czy obronie przed stresem oksydacyjnym. Im trudniej bakteriom pozyskać żelazo, tym więcej kosztuje je proces metaboliczny. Tym wolniej się też rozmnażają. W ludzkim organizmie najwięcej żelaza bakterie mogą pozyskać z hemu – związku, który jest kofaktorem hemoglobiny. Międzynarodowy zespół naukowców odkrył, że ingerencja w proces metabolizmu hemu, a tym samym żelaza, może skutecznie zwalczyć rozwój bakterii wielolekoopornych.
Bakterie wielolekooporne
ESKAPE to akronim określający grupę lekoopornych bakterii, do której zalicza się: Enterococcus faecium, Staphylococcus aureus, Klebsiella pneumoniae, Acinetobacter baumannii, Pseudomonas aeruginosa i Enterobacter spp. Bakterie P. aeruginosa oraz S. aureus powszechnie występują w biofilmie rany. Mogą prowadzić do wielu zakażeń, w tym infekcji płuc (jako pneumonia), krwi, dróg układu moczowego i innych ran pooperacyjnych. Po wejściu do środowiska organizmu ludzkiego uodparniają się na działanie antybiotyków. Ich leczenie staje się wtedy trudniejsze.
Oszukać bakterie
Naukowcy udowodnili, że podanie porfiryny galu (gallium porphyrin), który swoją budową przypomina hem, ale nie zawiera żelaza, wykazuje skuteczne właściwości antybakteryjne. Porfiryna galu to związek chemiczny, który mimetycznie naśladuje budowę hemu. Pozwala oszukać bakterie, które wchłaniają go w ramach metabolizmu hemu. Porfiryna galu szybko zabija gram-pozytywne i gram-negatywne szczepy bakterii, nawet te, które są wielolekooporne. Ponadto porfiryna galu jako znakomity fotouczulacz może zostać wykorzystana w terapiach fotodynamicznych.
Terapia fotodynamiczna (PDT)
Fotouczulacze, zwane także fotosensybilizatorami, pod wpływem promieniowania o określonej długości fali niszczą niepożądane struktury w organizmie. Terapia stosowana jest zazwyczaj w środowisku bogatym w tlen. Energia z fotonów jest absorbowana przez fotouczulacze i przesłana do otaczających molekuł. W efekcie powstają reaktywne formy tlenu i wolne rodniki, które mogą zniszczyć białka, lipidy i kwasy nukleidowe bakterii, co prowadzi do ich zabicia. W przeciwieństwie do antybiotyków, PDT nie wywołuje mutacji szczepów bakterii. Z tego powodu rozwój nowych technik terapii fotodynamicznych jest niezwykle atrakcyjny dla naukowców.
Zakażenia szpitalne
Stosowanie dużych ilości leków oraz zła polityka w środowisku szpitalnym doprowadziły do wyrobienia u bakterii mechanizmów obronnych przed działaniem dostępnych antybiotyków. Przepisywane w sposób nadmierny i nieukierunkowany antybiotyki często funkcjonują także w nieudokumentowanym obiegu i są przyjmowane w niewłaściwy sposób. Infekcje wywołane przez lekooporne patogeny są istotnym czynnikiem zagrażającym pacjentom w trakcie leczenia szpitalnego. Oporne bakterie stanowią również poważne wyzwanie w leczeniu ran. Dużą przeszkodą jest zdolność drobnoustrojów do wytwarzania biofilmu w ranie.
Biofilm jest złożonym skupiskiem jednego lub wielu gatunków drobnoustrojów, które pokryte są macierzą stanowiącą fizyczną barierę chroniącą bakterie przed działaniami zwalczającymi – antybiotykami, niektórymi antyseptkami oraz układem odpornościowym gospodarza. Biofilm kształtuje się w przeciągu kilku minut, a dojrzałość osiąga po około 48-72 godzinach.
Biofilm negatywnie wpływa na proces gojenia – przyczynia się do powiększenia obszaru rany, a także może prowadzić do powstawania martwicy trudnej do usunięcia. Biofilm stanowi również poważne zagrożenie dla życia i zdrowia pacjenta, gdyż może powodować zakażenie ogólnoustrojowe, np. sepsę.
Źródła: Uniwersytet Gdański, Laser Therapy. 2018 Dec 31; 27(4): 293–302, Biotechnologia.pl, Chemical Engineering Journal Vol. 451, Part 1, 1 Jan 2023